우리는 그동안 전자공학과 반도체의 역사에 대해서 살펴보았고, 반도체가 무엇인지 그 성질에 대해서 공부했으며, 양자역학을 이용한 띠이론(band theory)에 대해서까지 짚어보았습니다. 이 띠이론은 앞으로 반도체 특성을 설명할 때 단골로 등장할 것이므로 잘 이해를 하는 것이 좋겠고, 이해가 잘되지 않는다면 3월호를 다시 정독하면 도움이 되리라 생각합니다.
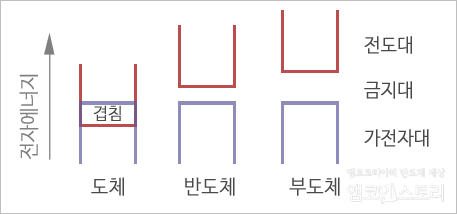
전기를 잘 흐르게 하는 도체, 잘 흐르지 못하게 하는 부도체, 때에 따라서 전기를 흐르도록 또는 흐르지 않도록 할 수 있는 반도체를 띠이론으로 설명할 수 있습니다. 도체의 경우에는 가전자대(전자가 채워져 있는 띠)와 전도대(비어있는 띠)가 겹쳐 있어서 많은 수의 전자가 띠사이를 쉽게 이동할 수 있으므로 큰 전류를 흐르게 합니다.
반도체와 부도체는 띠구조가 비슷하게 생겼는데, 가전자대와 전도대가 떨어져 있습니다. 이때, 떨어져 있는 두 띠의 사이를 금지대라고 부릅니다. 하지만 두 띠의 간격이 반도체의 경우에는 2.5eV 이하로 좁아서 (대표적인 반도체 물질인 규소의 경우는 1.11eV의 띠간격을 가지고 있습니다) 이 이상의 에너지를 공급하면 가전자대에 있는 전자들이 전도대로 뛰어 올라가 전류를 흐르게 할 수 있습니다.
다이아몬드를 예로 들면 5.48eV의 띠간격을 갖는데, 반대로 부도체는 두 띠의 간격이 커서 가전자대의 전자를 전도대에 올리기 매우 어려워 전류가 흐르지 않습니다. 그런데 앞에 묘한 단위가 등장했지요? eV란 전자볼트라고 부릅니다. ‘전자 하나가 1볼트의 전위를 거슬러 올라가는데 드는 일’이라고 정의되어 있습니다. 전자 하나도 별거 아니고 1볼트(꼬마전구를 켜는 건전지는 1.5볼트)도 별거 아니라고요? 하지만 1eV를 열로 환산하면 대략 1만도 정도 된다는 사실!
요약하자면, 도체는 금지대가 없고 반도체와 부도체는 금지대가 존재합니다. 그중 반도체는 금지대가 좁고 부도체는 넓다고 이해하면 되겠습니다.
▲ 도체, 반도체, 부도체의 띠 ⓒ백종식
이번에는 반도체의 띠구조에 대해서 아주 조금만 깊이 들어가 볼까요?
지금까지는 전자가 에너지를 얻어 가전자대로부터 전도대로 뛰어 올라가는 것만 고려했는데, 사실은 그 반대의 경우도 생각해볼 수 있습니다. 즉, 전도대에 있던 전자가 가전자대로 내려오면서 에너지를 방출하는 것 말이지요. 지난 3월호에서 이상한 호텔에서 손님이 객실을 바꾸는 예시를 들었습니다. 낮은 층에서 높은 층의 방으로 이동할 때 숙박료 차액을 내야 하고, 거꾸로 높은 층에서 낮은 층의 방으로 이동할 때 숙박료 차액을 돌려받는다고 했던 것을 생각하면 됩니다.
이때 방출되는 에너지는 빛의 형태가 되지만, 띠간격 크기에 따라 빛의 종류가 다릅니다. 대략 2eV에서 3eV 사이의 띠간격을 가지면 우리 눈에 보이는 가시광선 형태의 빛을 방출하게 되고 그보다 띠간격이 크면 자외선 형태의 빛을, 작으면 적외선 형태의 빛을 방출합니다. 최근 LED TV의 백라이트나 LED 조명등에 쓰이는 LED가 바로 이 원리를 이용한 것이지요.
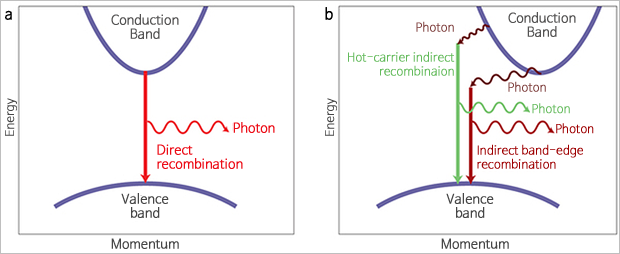
앞서 설명한 띠형태는 이해를 돕기 위해 필자가 간략하게 그린 것입니다. 실제로는 좀 더 복잡하게 생겼습니다. 전자가 띠사이를 이동할 때는 전도대의 가장 낮은 부분에서 가전자대의 가장 높은 부분으로 이동하게 됩니다. 아래 그림을 보면, 왼쪽 그림은 전도대의 가장 낮은 부분과 가전자대의 가장 높은 부분이 잘 정렬되어 있지만, 오른쪽은 전도대의 가장 낮은 부분이 오른쪽으로 치우쳐져 있지요. 왼쪽은 전자가 이동할 때 위에서 아래로 수직으로 이동하면 되지만, 오른쪽은 왼쪽으로 수평이동한 후에 수직으로 이동해야 합니다. 이때 수직으로 이동할 때는 빛을 방출하고 수평으로 이동할 때는 열을 방출합니다.
LED 등 빛을 내는 용도로 사용되는 반도체는 주로 왼쪽 그림과 같은 띠구조를 가지고 있습니다, 오른쪽 그림과 같은 띠구조를 갖는 반도체를 사용하여 LED 등을 만들면, 공급해준 전기에너지 일부가 열을 내는 데 사용되느라 빛을 내는 효율이 낮기 때문에 잘 사용하지 않습니다. 왼쪽 그림의 띠구조를 갖는 반도체를 직접천이 반도체라고 부르고 오른쪽 그림의 띠구조를 갖는 반도체를 간접천이 반도체라고 부릅니다.
▲ 직접천이 반도체와 간접천이 반도체의 띠구조
사진 출처 : http://goo.gl/wC7ekg
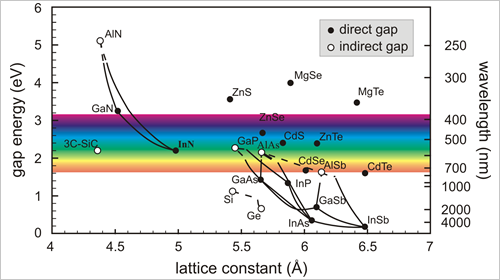
반도체 물질은 규소만 있는 것이 아니라 사실 꽤 많습니다. 어떤 물질은 직접천이 반도체(direct gap)이고, 어떤 물질은 간접천이 반도체(indirect gap)입니다. 검은색 점으로 표시된 반도체 물질들 중에서 윗부분에 있는 것들은 자외선 빛을 내는 반도체 물질로, 이 중에서 GaN는 LED 조명등이나 LED TV의 광원으로 많이 사용합니다.
▲ 반도체의 종류
사진 출처 : http://goo.gl/GZATCp
위의 그림에서는 몇 가지 반도체 물질을 보여주고 있습니다. 먼저 규소와 게르마늄 등 홑원소로 된 것들과 갈륨비소(GaAs), 인듐인(InP)처럼 두 가지 원소로 구성된 화합물 형태의 반도체 물질들이 있고, 심지어 세 가지 이상의 원소로 구성된 화합물 반도체도 있습니다. 이 다양한 반도체 물질들은 여러 응용분야에 따라서 사용되고 있습니다.
특히, 이 중에서 규소가 반도체의 대표 주자로서 가장 많이 사용되고 있데요, 그 이유가 무엇일까요? 중학교 과학 시간에 우리가 배운 바로, 지각을 이루는 8대 원소가 있었습니다. 종종 시험문제에 나와서 우리를 괴롭히곤 했던 것이었지요. ‘오시알페카나크마’라는 단어를 무조건 외웠던 기억이 나네요. 풀어서 쓰면, ‘O, Si, Al, Fe, Ca, Na, K, Mg’이며, 산소, 규소, 알루미늄, 철, 칼슘, 나트륨, 칼륨, 마그네슘 순으로 많다는 뜻입니다. 즉, 지구 땅덩어리를 구성하는 물질 중 가장 많은 것이 산소를 제외하고는 바로 규소라는 것이지요. 당연히 규소는 값싼 원재료가 되겠지요? 정말 흙 퍼서 돈 번다는 것이 말이 되네요! 절연체를 만들기 쉽다는 점과 다른 좋은 특성들이 있어서 규소가 반도체의 챔피언이 된 것인데요, 여기서는 굳이 다루지는 않겠습니다. 그럼 다음 주에 뒷이야기를 계속 이어가겠습니다.